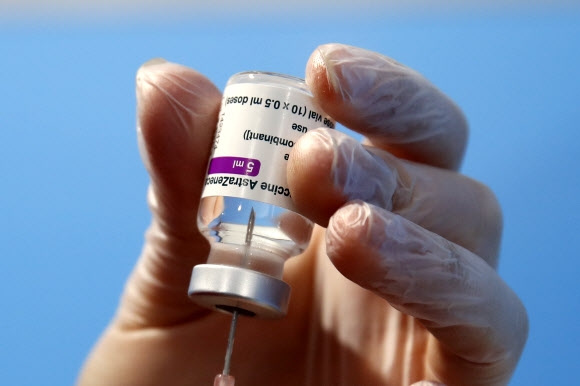
‘아나필락시스’ 등 코로나19 백신 접종 이상반응 얼마나?
급성 안면마비, 화이자 4건-모더나 3건대부분은 통증·피로감·두통 등 경미해
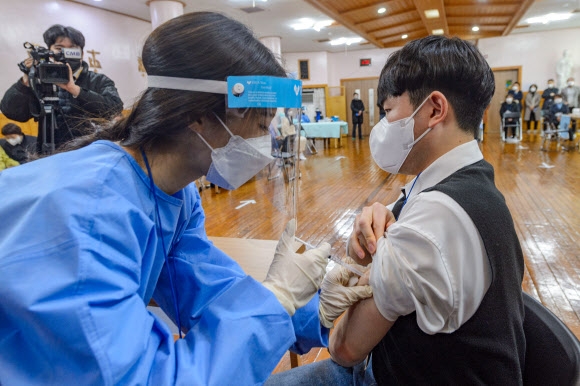
오는 26일 국내에서 코로나19 백신 접종이 시작되는 가운데 접종 후 이상반응에 대해 관심이 모아지고 있다.
백신 접종이 시작되면 접종 부위 통증, 두통, 근육통, 피로감 등의 이상반응은 흔하게 나타날 것으로 예상된다.
해외에서 진행된 임상시험 등에서는 적지 않은 접종자들에게 통증, 부기, 발적 등 국소반응과 발열, 피로감, 두통, 근육통 등 전신반응이 나타났다.
다만 이런 증상이 반드시 백신 접종에 의한 것이라고는 볼 수 없다.
아나필락시스 화이자 100만명당 11.1명…모더나 2.4명이상반응 중 가장 관심을 가져야 할 증상은 접종 후 몇 분, 또는 몇 시간 내에 전신에 일어나는 중증 알레르기 반응인 ‘아나필락시스’다.
아나필락시스는 해외에서 드물기는 했지만 일부 발생했다.
화이자 백신 접종군에서는 100만명당 11.1명, 모더나 접종군에서는 100만명당 2.4명의 비율로 나타났다.
미국에서는 두 가지 백신과 관련해 7건의 급성 안면마비도 있었다.
아스트라제네카 백신 접종군에서는 아나필락시스는 없었고, 인과성이 명확하지는 않지만 횡단성척수염이 1건 보고됐다.
아나필락시스는 접종 후 몇 분 안에도 발생하기 때문에 접종이 끝나면 최소 15분간 의료기관에 머물면서 증상 발생 여부를 살펴봐야 한다.
아나필락시스는 알레르기 치료제인 에피네프린을 즉각 투여하면 호전된다.
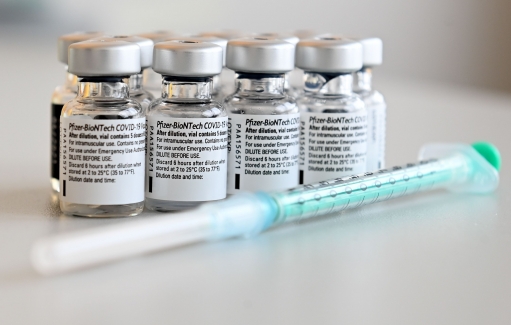
화이자 백신, 아나필락시스 100만명당 11.1명23일 코로나19 예방접종 대응 추진단이 공개한 코로나19 임상시험 결과자료를 보면 화이자 백신 임상참여자에게는 ▲접종 부위 통증(84.1%) ▲피로감(62.9%) ▲두통(55.1%) ▲근육통(38.3%) ▲오한(31.9%) ▲관절통(23.6%) ▲접종부위 부기(10.5%) ▲발적(9.5%) ▲메스꺼움(1.1%) ▲권태감(0.5%) ▲림프선염(0.3%) 등의 이상반응이 있었다.
흔하게 나타나는 증상 외에는 급성 안면마비가 4건 보고됐다.
알레르기 반응은 임상 후 대규모 예방접종을 하는 과정에서 보고됐다.
미국에서는 지난해 12월 14~23일 보건의료인 등 189만여명이 화이자 백신을 맞았고, 이 가운데 0.2%(4393명)가 알레르기 반응을 보였다.
이 중 175명은 중증일 가능성이 있어 정밀 검토한 결과 아나필락시스는 21명이었고 비(非)아나필락시스 알레르기 반응은 83명이었다.
나머지는 알레르기와 상관없이 실신하거나 불안증세를 보인 경우였다.
아나필락시스 발생률은 100만명당 11.1명이었다. 이들 21명 중 17명은 과거에 알레르기나 알레르기 반응을 경험한 적이 있었고, 7명은 아나필락시스를 겪은 적이 있었다.
15명은 접종 후 15분 이내에, 3명은 15∼30분 사이에, 3명은 30분 이후에 증상이 나타났다. 신상 추적이 가능했던 20명은 모두 회복했다.
비아나필락시스 알레르기 반응자 83명 중 56명도 과거 약물이나 음식에 알레르기가 있었다.
모더나 백신, 아나필락시스 100만명당 2.5명모더나 백신 임상 과정에서는 ▲접종부위 통증(92.0%) ▲피로(70.0%) ▲두통(64.7%) ▲근육통(61.5%) ▲관절통(46.4%) ▲오한(45.4%) ▲메스꺼움·구토(23.0%) ▲겨드랑이 부위 부기·압통(19.8%) ▲발열(15.5%) ▲접종부위 종창(14.7%) ▲접종부위 홍반(10.0%) 등이 주로 관찰됐다.
임상에서는 백신과의 인과성이 확실하지 않은 3건의 급성안면 마비도 있었다.
미국에서는 모더나 접종이 시작된 이후 알레르기 반응이 관찰됐다.
지난해 12월 21일부터 올해 1월 20일 사이에 모더나 백신을 맞은 404만여명 중 0.03%(1266명)에서 알레르기 반응이 나타났고, 이 중 108명이 중증으로 의심됐다.
108명 중 10명은 아나필락시스였고, 발병률은 100만명당 2.5명이다. 43명은 비아나필락시스 알레르기 반응이었다.
아나필락시스 10명 중 9명은 과거 알레르기를 겪은 적이 있었고, 5명은 백신과 무관하게 아나필락시스를 경험한 적이 있었다.
아나필락시스가 생긴 시점은 접종 후 15분 이내가 9명, 30분 이후가 1명이었다. 10명 모두 치료제인 에피네프린을 맞았고, 추적 관찰이 가능한 8명은 모두 회복했다.
비아나필락시스 알레르기 반응을 보인 43명은 가려움증, 발진, 입과 목에 간지러운 느낌, 목이 막히는 느낌, 호흡기 증상 등을 주로 호소했고, 이 중 26명은 과거 약물이나 음식에 알레르기를 보인 사람들이다.
AZ 백신, 아나필락시스 없고 횡단성척수염 1건 보고아스트라제네카 백신 임상에서 보고된 이상반응은 ▲접종부위 압통(60% 이상) ▲접종부위 통증·두통·피로감(50% 이상) ▲근육통·권태감(40% 이상), ▲발열·오한(30% 이상) ▲관절통·오심(20% 이상) 등이었다.
대부분의 이상반응은 경도에서 중증도 수준이었다. 대부분은 수일 내에 없어졌고, 7일까지 지속된 경우는 국소 반응이 4%, 전신반응이 13% 정도였다.
2차 접종에서 보고된 이상반응은 1차에 비해 경미하고 빈도도 낮았다.
식품의약품안전처가 지난 1일 발표한 아스트라제네카 백신 검증 자문단 회의결과에 따르면 영국과 브라질, 남아프리카공화국에서 수행된 임상시험에서는 중증의 이상 사례가 보고됐다.
임상에는 백신군 1만 2021명, 대조군 1만 1724명 등 총 2만 3745명이 참여했는데 백신군 0.7%(79명), 대조군 0.8%(89명)에서 중대한 이상 사례가 발생했다.
백신군에서 발생한 중대 이상 사례로는 발열(1건)·횡단성척수염(1건) 등이 있었다. 그러나 아나필락시스나 코로나19 증상 악화 등은 없었다.
즉 과거에 아나필락시스는 물론 약물이나 음식에 알레르기를 겪은 접종자는 접종 후 15~30분간 의료기관에 머무르면서 경과를 지켜볼 필요가 있다.
신진호 기자 sayho@seoul.co.kr






![[열린세상] ‘백신 접종 이후’의 세계는/하대청 광주과학기술원 기초교육학부 교수](https://img.seoul.co.kr/img/upload/2018/08/05/SSI_20180805184335_V.jpg)

![[속보] 총리 “아스트라제네카 백신 안전 문제 없다”](https://img.seoul.co.kr/img/upload/2020/12/27/SSI_20201227181824_V.jpg)


![[고든 정의 TECH+] 스스로 생분해되는 3D 프린팅 스텐트 (연구)](https://imgnn.seoul.co.kr/img/upload/2021/02/14/SSI_20210214181819_V.jpg)